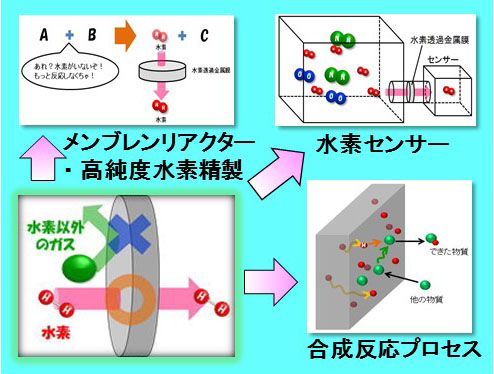
「水素透過金属膜(すいそとうかきんぞくまく)」は水素だけが通りぬけることができる金属の膜です。その特性を活かして、とてもキレイな水素をつくることができます。
ところで、何かが膜を通りぬけるときには、その膜に小さな穴、「細孔(さいこう)」があって、そこを通りぬけると考えるのが自然ですね。しかし、今回紹介する水素透過金属膜は、小さな穴なんて存在しないのに、水素が通りぬけることができるのです。とても不思議ですね♪
なんでそんなことが起こるのでしょうか?
まずは水素が金属を通りぬける様子を示している下の動画と画像をごらんください。
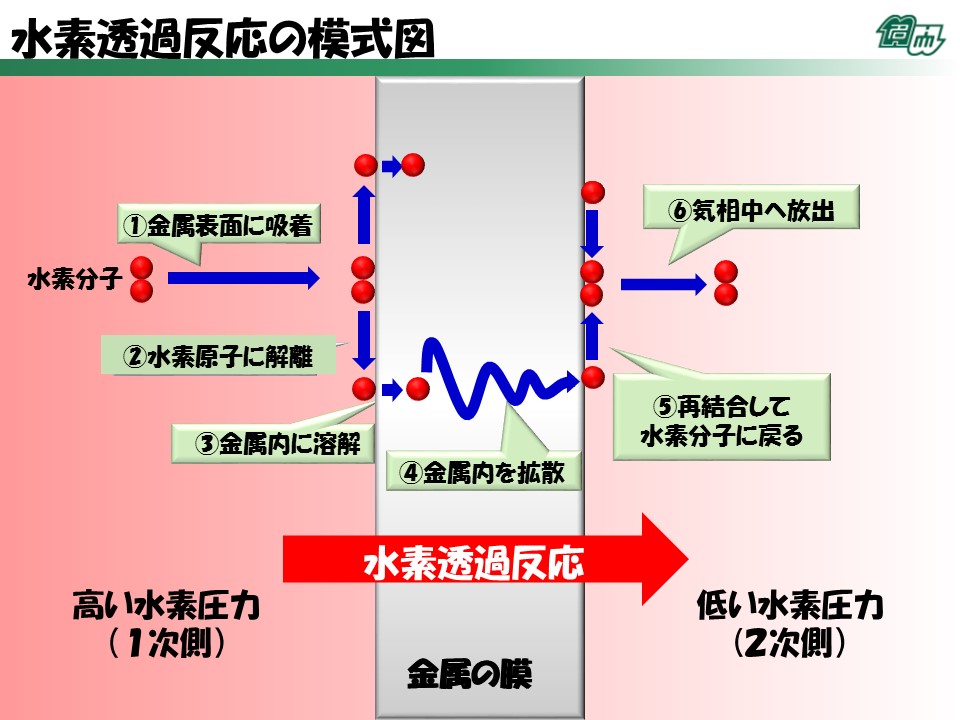
これが水素が金属の中を通りぬけるときに起こっていることです。
まず水素は動画や画像に示された赤い球2つのように、水素原子(球1個分)が2つくっついた水素分子として存在しています。皆さんが吸っている空気には、窒素や酸素が含まれていますが、これらもそれぞれ窒素原子や酸素原子が2つくっついていて、それらがとてもたくさんそこら中を飛び回っているのです。
簡単にいうと、目に見えないほど小さな原子のカップルが2人で手をつないで仲良くデートしている感じです。
さて、今この水素のカップル(水素分子)が水素透過金属膜の前にやってきました。水素はまず金属の表面にくっつきます。これを「吸着(きゅうちゃく)」といいます。吸着した水素のカップルは、そこでなんと手を離してしまうのです!そうです、お別れです。寂しいですね。このお別れのことを「解離(かいり)」といいます。
お別れをした水素原子は、それぞれ金属の中に入りこみます。これを「溶解(ようかい)」といいます。さっきこの膜は穴がないって言ったのに、水素が入りこむのはおかしいと思いましたか?そうですね。
それでは、ここで少しだけ金属について見てみましょう。下の図をごらんください。
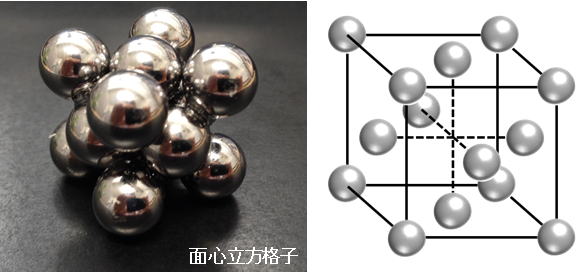
金属の中では図のように、金属の原子が決まった形できれいに並んでいます。
このように原子がきれいに並んでできた物質を「結晶(けっしょう)」といいます。実際には、上の図のような決まった形「単位格子(たんいこうし)」がたくさん集まっているのです。
上の例は「面心立方格子(めんしんりっぽうこうし)」と呼ばれる単位格子で、立方体の角とそれぞれの面の中心に原子があります。
さらに結晶の中を詳しく見てみましょう。下の図をごらんください。

この図はさきほどの面心立方格子を上から見た図で、隣にもう1つくっついたものです。
面心立方格子は立方体の中心に原子がないので、写真のように「すきま」ができます。水素原子はこうした「すきま」に入りこむのです。これが溶解のメカニズムです。
この「すきま」はいわゆる穴に比べるととても小さいので、水素以外の原子はほとんど入りこむことができません。よってこの時点水素以外の原子はほとんどいなくなるのです。
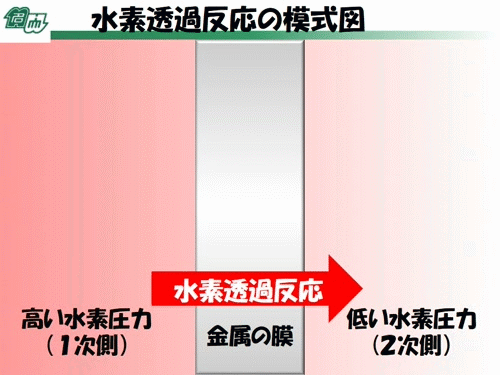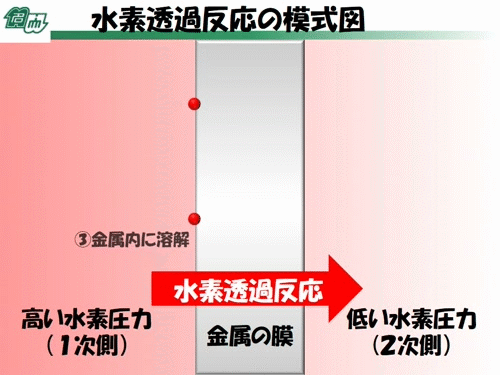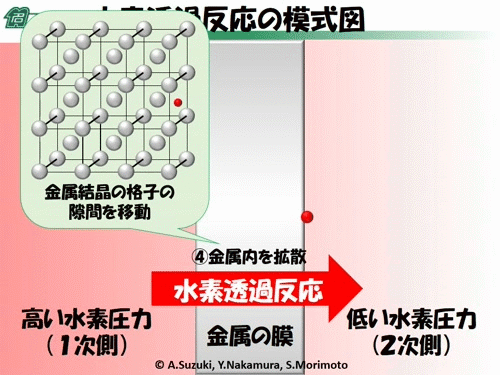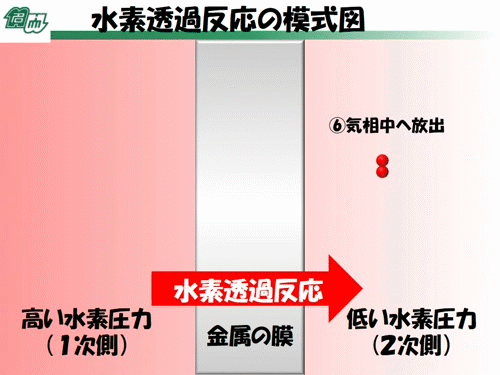
金属内に溶解した水素はそこでじっとしているわけではありません。
真ん中から右の写真のように、「すきま」から隣の「すきま」へと移動し、それを繰り返すことで一歩一歩進んでいきます。
このことを「拡散(かくさん)」といいます。
膜を通りぬける間におよそ1万回から10万回ほど、「すきま」から隣の「すきま」への移動を繰り返します。
さきほど、溶解のときに少しだけ入りこんだ他の物質は、拡散が水素に比べるととてつもなく遅いので、水素の移動についてこられません。
このように、溶解と拡散の2つのプロセスで水素と他の物質を分け、きれいな水素を作り出すのが水素透過金属膜の特徴です。
そして拡散を終え、膜の反対側へたどりついた水素原子はもう1人と再会を果たします。そして、再び手をつなぐのです。
これを「再結合(さいけつごう)」といいます。
無事カップルに戻った水素は金属からはなれます。これを「放出(ほうしゅつ)」といい、そこはもう水素しかいない世界です!
 |
☆ ポイント 「水素透過金属膜」は、水素だけが通りぬけられる金属の膜である。 金属原子のすきまに水素が入り込む「溶解」と、すきまからすきまに移動する「拡散」によって、 水素だけが膜を通りぬけ、とてもキレイな水素をつくることができる。 |